Le docteur Docteur Hajar NAIMI est médecin dans le service de Chirurgie générale - digestive - vasculaire - thoracique et endocrinienne.


Le docteur Docteur Hajar NAIMI est médecin dans le service de Chirurgie générale - digestive - vasculaire - thoracique et endocrinienne.

Face à la progression inquiétante de l’obésité et du diabète chez les enfants et adolescents, le Luxembourg a créé le 24 mai 2024 OBEDIA-Kids, un réseau national de compétences en diabète et obésité sévère. Il rassemble trois partenaires clés : le Centre Hospitalier de Luxembourg (CHL), les Hôpitaux Robert Schuman (HRS) et le Rehazenter. Sa mission : prévenir, dépister et coordonner la prise en charge des jeunes patients au sein d’un cadre structuré et collaboratif. Le lancement officiel du réseau aujourd’hui marque une avancée majeure pour la santé des enfants et adolescents au Luxembourg.
La première rencontre conjointe entre les représentants officiels du Réseau de Compétence OBEDIA-Kids a eu lieu le 22 octobre 2025. Le réseau de compétences est piloté par différents collectifs, chacun disposant de missions spécifiques, et qui constituent les organes de gouvernance du réseau. Ce jour, le Comité de Gestion (CdG) et le Conseil Scientifique (CS) se sont réunis pour discuter de l’avancée de la mise en place.
« Au Luxembourg, parmi les maladies non-transmissibles (NCD’s) chez les enfants, l’obésité et le diabète nécessitent une prise en charge multidisciplinaire à vie. Aujourd’hui, un enfant sur cinq est en surpoids ou en obésité. 60 à 80 % d’entre eux le resteront à l’âge adulte, et présenteront des complications physiques, psychologiques et sociales importantes et un risque augmenté de développer un diabète insulino-résistant (de type 2, en relation avec une obésité). Parallèlement, le diabète de type 1, qui lui est insulino-déficient (manque absolu d’insuline) et alors potentiellement mortel sans traitement par injections d’insuline, croît de 2 à 3 % chaque année. Les enfants présentant un diabète type 1 ou une obésité ont besoin d’un suivi régulier et d’un accompagnement renforcé lors de la transition vers la prise en charge dans les services adultes. Grâce à la mise en place de notre Réseau de Compétences, nous espérons pouvoir améliorer l’accompagnement de ces enfants et adolescents pour une meilleure gestion de leurs maladies à l’âge adulte. », explique le Dr Carine De Beaufort, médecin spécialiste en pédiatrie, diabétologie et endocrinologie au CHL.
Les principaux objectifs d’OBEDIA-Kids sont de renforcer la coopération entre les acteurs hospitaliers, libéraux et institutionnels afin de fluidifier les parcours de soins, et d’améliorer ainsi que d’évaluer la qualité des prises en charge grâce à des outils adaptés à chaque pathologie.
Le réseau se concentre principalement sur deux axes : l’obésité pédiatrique, en favorisant une collaboration étroite entre le SNPJ, le Rehazenter et les professionnels de santé libéraux (pédiatres, diététiciens, psychologues), et le diabète de l’enfant, en garantissant une coordination entre les services pédiatriques et les équipes adultes pour assurer une transition sécurisée à l’adolescence.
Par ailleurs, OBEDIA-Kids est un SWEET Centre de Référence de diabétologie pédiatrique (SWEET initiative, www.sweet-project.org) et membre de l’ERN (Réseau de Référence Européen) Endo (endocrinologie pédiatrique rare), ce qui lui permet de bénéficier d’un niveau d’expertise international et de favoriser le partage de bonnes pratiques entre centres spécialisés.
Les partenaires clés
OBEDIA-Kids s’appuie sur une collaboration étroite entre trois institutions :
Se rajoutent à cette collaboration les partenaires libéraux, les pédiatres, médecins généralistes, les diététiciennes et psychologues, nécessaires pour établir un vrai réseau pour la prise en charge des enfants avec cette pathologie chronique , complexe.
Cette organisation permet de réunir les compétences médico-soignantes, psychologiques et diététiques indispensables à une prise en charge complète et adaptée à chaque enfant.
This scoping review was conducted to better understand how digital health technologies support patient empowerment in people with chronic diseases. Specifically, we aimed to identify which aspects of empowerment are enhanced by digital health technologies, and what barriers or facilitators influence this process.
We sought to answer three main questions:
What aspects of patient empowerment are most valued by people with chronic diseases when using DHTs?
How do DHTs support the empowerment of patients?
What factors influence the attainment of empowerment when using DHTs?
We identified nine recurring empowerment aspects, which were grouped into three overarching and interrelated empowerment dimensions supported by digital health technologies: health information and knowledge management, self-management, and emotional and social support.
Digital health technologies supported these empowerment dimensions through various functional components such as informing patients, allowing communication with the health care team, patient monitoring, behavior change interventions, individualized feedback, or peer support, each contributing to a varying degree.
The degree of empowerment varied based on personal, social, technological and environmental factors, including: demographic and socioeconomic status, digital literacy, disease status, perceived value of technology, sociocultural values and norms, doctor-patient relationship, connectivity, and cost influenced the development of empowering capabilities resulting from using DHTs.
Our finding offers a patient-centered framework for understanding patient empowerment and its process. This framework can serve as a practical guide for technology developers in designing tools that genuinely empower patients, for researchers in evaluating digital interventions through an empowerment-oriented lens, and for healthcare stakeholders in promoting equitable and meaningful patient participation in care.
Original article: Empowering capabilities of people with chronic condition in the context of digital health technologies: a scoping review, Fomo M., Borga L.G., Abel T., Santangelo P.S., Riggare S., Klucken J., Paccoud I., J Med Internet Res 2025;27:e68458, doi: 10.2196/68458, PMID: 40577044, PMCID: 122547

Dr JOCHEN KLUCKEN
More information:
https://pubmed.ncbi.nlm.nih.gov/40577044/

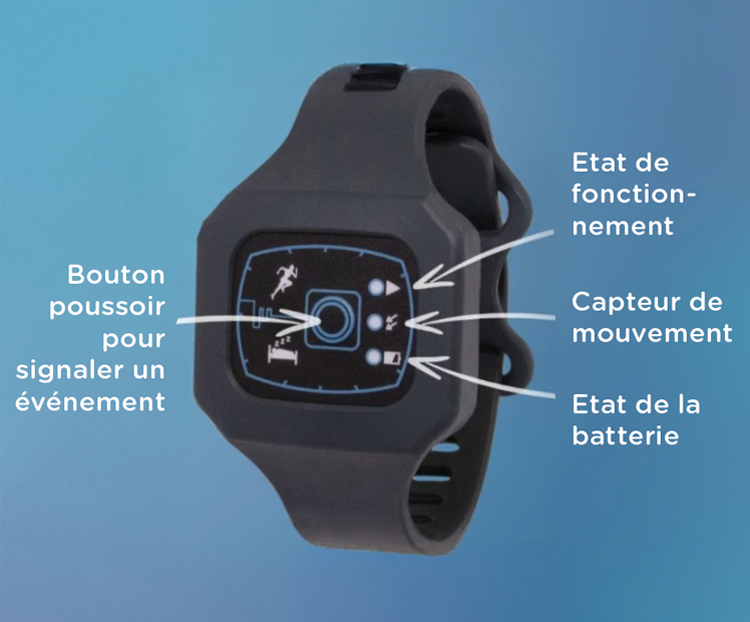
Un actimètre de poignet est un dispositif médical sous forme d’un bracelet ou d’une montre permettant de mesurer et d’analyser les mouvements d’un patient pendant plusieurs jours/nuits consécutifs à domicile. Les enregistrements ont pour objectif d’analyser le rythme veille-sommeil du patient nécessaires à la pose du diagnostic et le traitement des troubles du sommeil.
L’actimètre est un petit appareil qui se porte au poignet tel qu’une montre/bracelet, il comporte un capteur qui permet d’enregistrer les mouvements du poignet et l’activité motrice du patient. Les données collectées sont ensuite transférées à un ordinateur pour analyse et interprétation par un médecin spécialiste.
Quand vous débutez l’actimétrie :
1. Mettez l’actimètre au bras non dominant.
2. Gardez-le au poignet en fonction de la durée définie par le médecin.
3. Pressez le bouton au coucher et au lever ainsi que lors d’un éveil ou événement nocturne.
4. Remplissez le calendrier de sommeil comme cela vous a été expliqué lors de la remise de l’actimètre.
À la fin de l’examen :
1. Retirez l’actimètre à votre réveil.
2. Rapportez-le à l’hôpital.
Le calendrier du sommeil se remplit tout au long de la journée en faisant des annotations régulières, conformément à la durée définie par le médecin et en parallèle d'une actimétrie.
Voici un exemple de remplissage du calendrier du sommeil :
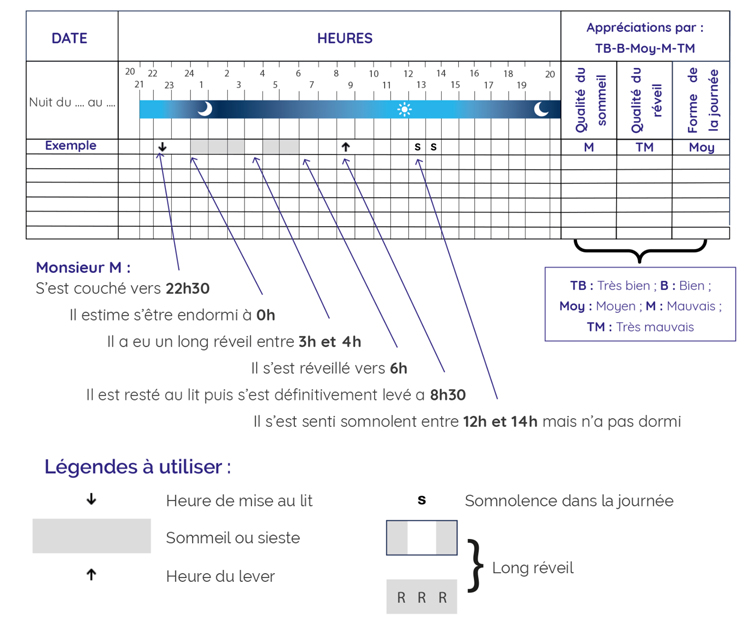
ATTENTION :

Nous avons le plaisir de vous informer qu’à partir de janvier 2026, le CHL Praxiszentren Grevenmacher élargit son offre de soins et devient une véritable antenne hospitalière de proximité, pensée pour vous accueillir dans un cadre agréable, moderne, et facilement accessible, sans avoir à vous rendre à l’hôpital.
Ainsi, vous pourrez-vous détendre et vous sentir pleinement à l’aise avant, pendant et après votre consultation ou traitement.
Notre objectif est de vous proposer une prise en charge plus proche de chez vous, tout en maintenant les mêmes standards de qualité, de sécurité et de continuité des soins qu’à l’hôpital.


Grâce à cette nouvelle infrastructure, vous profiterez d’un accompagnement personnalisé dans un lieu moins institutionnel, sans compromis sur l’excellence médico-soignante ni sur l’expertise de nos équipes.
Vous pourrez également profiter de nombreuses places de parking disponibles à proximité immédiate, facilitant grandement votre venue.


Le CHL s’est mobilisé autour de la santé masculine avec une journée riche en sensibilisation et en échanges. Dès le matin, une prostate et une vessie géantes installées dans le hall ont attiré l’attention des visiteurs : un dispositif pédagogique qui a permis d’expliquer de manière concrète les pathologies les plus fréquentes de ces organes. L’équipe a joué le jeu avec une photo collective moustachue, symbole de l’engagement autour de MOVEMBER.

La soirée s’est poursuivie avec une conférence complète couvrant les grands enjeux de santé masculine :


Moment fort de la soirée :
Le témoignage profondément humain de M. Bernard Vidali, patient et auteur du livre « Courage et vérité – Histoire de mon cancer », présenté en collaboration avec Mme Vanessa Grandjean, psychologue spécialisée en oncopsychologie. Un récit sincère, lucide et porteur d’espoir, qui a particulièrement touché le public.


Une journée qui rappelle l’importance du dépistage, de l’information et du soutien, au cœur même de l’esprit MOVEMBER.


Depuis janvier 2026, il est possible de prendre rendez-vous CHL pour une mammographie de dépistage dans le cadre du Programme du ministère de la Santé, au nouveau centre de mammographie de Grevenmacher, pour des dates à partir du mardi 6 janvier 2025.
Les mammographies de dépistage pourront toujours être réalisées à la Maternité du CHL.
Cependant, nous encourageons fortement les personnes invitées par le Programme national (45–74 ans) à se rendre au PRAXISZENTREN GREVENMACHER, spécialement conçu pour ce type d’examen et offrant un accès facilité.
CHL PRAXISZENTREN - GREVENMACHER
30, route de Trèves, L-6793 Grevenmacher
(Entrée via rue Schiltzenplatz)
Pour prendre rendez-vous dans le cadre du dépistage, vous devez être en possession d’une invitation officielle, comme illustré ci-dessous.

Prendre rendez-vous pour une MAMMOGRAPHIE DE DÉPISTAGE – PROGRAMME DU MINISTÈRE DE LA SANTÉ
Vous pouvez d'ores et déjà prendre rendez-vous pour une MAMMOGRAPHIE DE DÉPISTAGE PROGRAMME DU MINISTÈRE DE LA SANTÉ (DE 45 À 74 ANS) au PRAXISZENTREN GREVENMACHER en cliquant ici.
Les premiers rendez-vous sont disponibles à partir du 6 janvier 2026.
Les autres examens d’imagerie du sein : mammographies diagnostiques, échographies mammaires, examens interventionnels,... restent effectués dans le service de Mammographie - Sénologie à la Maternité du CHL, uniquement sur rendez-vous et sur présentation d’une ordonnance médicale.


Le Dr Cathy Feyder est médecin dans le service de traumatologue du CHL.

À l’occasion de la Journée mondiale des droits de l’enfance, célébrée ce 20 novembre, les équipes médico-soignantes de la Kannerklinik du CHL lancent une campagne de sensibilisation multilingue dédiée à la prévention des accidents domestiques chez les enfants.
Cette initiative vise à informer et sensibiliser les parents afin de réduire les risques d’accidents courants - brûlures, traumatismes intoxications, etc. - qui touchent encore trop fréquemment les jeunes enfants.
A travers une série de courtes vidéos témoignages, les professionnels de santé partagent, sur base de leur expérience et de leur expertise, les situations du quotidien à éviter afin de garantir la sécurité des enfants à la maison.
Dr Charlotte Pierron, médecin spécialiste en Néonatologie et Soins intensifs pédiatriques au CHL : « Cette campagne me tient particulièrement à cœur. Nous accueillons encore trop souvent aux urgences et aux soins intensifs des enfants victimes d’accidents qui auraient pu être évités grâce à quelques gestes simples de prévention. Notre objectif est d’aider les parents à adopter les bons réflexes pour protéger leurs enfants au quotidien. »